
Research
研究概要
岩﨑研究室では有機化学の研究を行っています。 有機合成を駆使して新しい分子を創り出すこと、遷移金属を中心に周期表上の様々な元素と組み合わせることで独自の分子の合成を行っています。 分子の機能、構造美、社会に役立つ可能性はあるか、など多角的な視点で新しくておもしろい化学を探求します。
1. 触媒の力で有機化学の常識を覆す

有機化学の授業で様々な反応を習いますが、反応式にはその反応に関与する部分(官能基)しか登場しません。しかし、もの作りの現場で取り扱う分子は複雑で官能基をいくつも持っています。
効率的なもの作りのためには望みの官能基を選択的に反応させる「化学選択性」が必要になります。これまでの有機化学では、最も反応性の高い(=反応の活性化障壁が低い)官能基を反応させることに主眼が置かれ、反応試薬や反応条件によって選択性の改善が図られてきました。
これに対して、より反応性の低い官能基を選択的に反応させることができれば、合成戦略を一変させるゲームチェンジャーになると、私たちは考えています。有機化学の常識に挑戦するための力強い武器になるのが「触媒」です。触媒は、遷移状態に作用することで反応の活性化障壁を下げることができるので、私たち独自の触媒設計によって、有機化学の常識に囚われることなく、狙った反応を選択的に起こすことを目指しています。また、触媒の候補となる遷移金属錯体の合成も行なっています。
1-1. 化学選択的な水素ガスを用いたカルボニル基の還元反応
水素ガスによってカルボニル化合物を還元する反応は実験室のみならず工業的にも重要な反応です。カルボニル化合物は、カルボニル炭素に結合する二つの置換基によって反応性が大きく異なることが知られています。異なるカルボニル化合物が共存するなかで、触媒によって化学選択的に狙ったカルボニル化合物を還元することに取り組んでいます。
例えば独自に開発したイリジウム触媒( 東京化成工業より市販)を用いると、カルボニル化合物の中で最も反応性が低いとされるウレアをホルムアミドとアミンへと変換できます。この反応ではエステルなどが共存してもウレア選択的に反応が進行します。この化学選択性は、一般的なカルボニル化合物の反応性の序列とは矛盾します。
すなわち、触媒によってカルボニル化合物の反応性の序列を覆すことができることを実証しました。
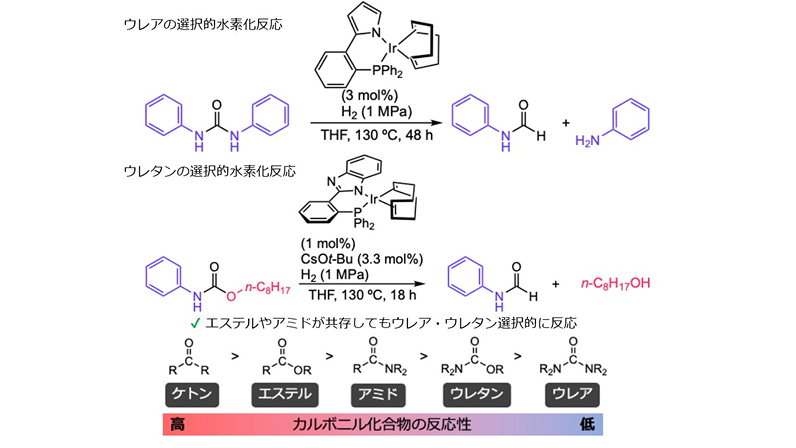
触媒と添加剤を工夫することでウレタンをホルムアミドとアルコールに変換することにも成功しました。この反応においてもエステルやアミドは水素化されることはありません。
ポリウレタンは自動車のシートやベッドのマットレスに使われている汎用の高分子材料です。近年、環境問題に関連して廃プラスチックのケミカルリサイクルが注目されています。我々は、独自の触媒を用いてポリウレタンの分解反応に取り組み、水素ガスによって分解できることを実証しました。エステルやアミドと反応することなくウレタン選択的に反応することから、ポリウレタンとポリエステルの混紡繊維などのリサイクルにも応用できると期待しています。
関連文献
T. Iwasaki, Y. Yamada, N. Naito, K. Nozaki, J. Am. Chem. Soc. 2024, 146, 25562–25568.
T. Iwasaki, K. Nozaki, Nat. Rev. Chem. 2024, 8, 518–534.
T. Iwasaki, N. Saito, Y. Yamada, S. Ajiro, K. Nozaki, Organometallics 2024, 43, 924–928.
T. Iwasaki, K. Tsuge, N. Naito, K. Nozaki, Nat. Commun. 2023, 14, 3279.
1-2. エーテルを用いたクロスカップリング反応
2010年にクロスカップリング反応がノーベル化学賞の対象になりました。クロスカップリング反応は、炭素と炭素を連結する強力な手法ですが、反応点として炭素―ハロゲン結合が必要となり、反応基質の入手が時として問題となっていました。エーテルは有機化合物に遍在する官能基ですので、エーテルをクロスカップリング反応の反応点とすることができればより有用です。ロジウム触媒を用いることでビニルエーテルの炭素―酸素結合の切断を伴ったグリニャール試薬とのクロスカップリング反応が効率よく進むことを明らかにしました。
興味深いことにクロスカップリング反応の反応点として多用される炭素―臭素結合があってもエーテルの炭素―酸素結合が優先的に切断されます。ベンゾフランのような酸素を含む芳香族化合物を反応基質としても炭素―酸素結合を切断できます。また、より安価な鉄触媒も同じ反応に触媒活性を示すことも明らかにしました。
関連文献
T. Iwasaki, W. Ishiga, S. Pal, K. Nozaki, N. Kambe, ACS Catal. 2022, 12, 7936–7949.
T. Iwasaki, R. Akimoto, H. Kuniyasu, N. Kambe, Chem. Asian J. 2016, 11, 2834–2837.
T. Iwasaki, Y. Miyata, R. Akimoto, Y. Fujii, H. Kuniyasu, N. Kambe, J. Am. Chem. Soc. 2014, 136, 9260–9263.
1-3. ハロゲンの脱離能を覆す触媒反応
有機化学で習う求核置換反応では塩化物イオン、臭化物イオン、ヨウ化物イオンが脱離基として登場しますが、同族のフッ化物イオンは登場しません。これは炭素―フッ素結合が、炭素が形成する単結合の中で最も強い結合だからです。実際に、テフロンは化学的に安定な高分子材料です。
これに対して、遷移金属とグリニャール試薬から生じる遷移金属に負電荷を有するアート型錯体を触媒として用いると、フッ化アルキルの炭素―フッ素結合の切断を伴ったクロスカップリング反応が進行することを明らかにしました。興味深いことに、塩化アルキルよりもフッ化アルキルが優先的に反応します。このようなハロゲンの脱離能の序列を覆す結果は、アート型錯体の特徴によるものです。対カチオンであるマグネシウムカチオンがフッ素原子と選択的に相互作用することでフッ化アルキル選択的に反応することを実験化学と理論科学計算によって明らかにしました。
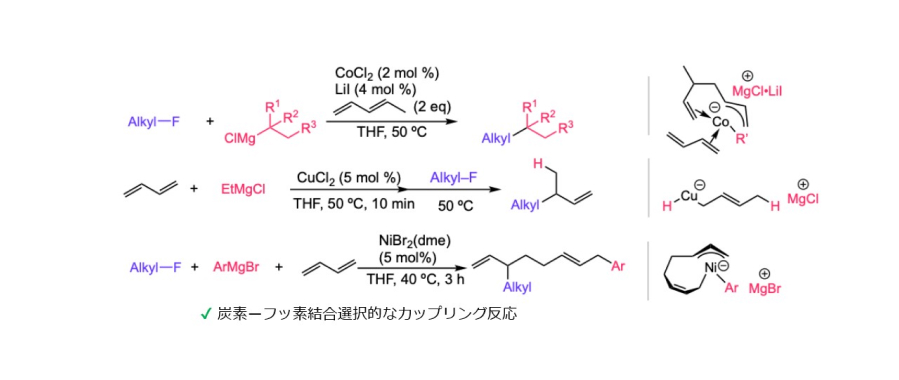
関連文献
T. Iwasaki, N. Kambe, Chem. Rec. 2023, 23, e202300033.
T. Iwasaki, 有機合成化学協会誌 2020, 78, 109–120.
T. Iwasaki, A. Fukuoka, W. Yokoyama, X. Min, I. Hisaki, T. Yang, M. Ehara, H. Kuniyasu, N. Kambe Chem. Sci. 2018, 9, 2195–2211.
T. Iwasaki, K. Yamashita, H. Kuniyasu, N. Kambe, Org. Lett. 2017, 19, 3691–3694.
T. Iwasaki, X. Min, A. Fukuoka, H. Kuniyasu, N. Kambe, Angew. Chem. Int. Ed. 2016, 55, 5550–5554.
T. Iwasaki, R. Shimizu, R. Imanishi, H. Kuniyasu, N. Kambe, Angew. Chem. Int. Ed. 2015, 54, 9347–9350.
T. Iwasaki, H. Takagawa, S. P. Singh, H. Kuniyasu, N. Kambe, J. Am. Chem. Soc. 2013, 135, 9604–9607.
2. 構造美を備えた分子の合成
あなたが美しいと思う分子はなにですか?
天然や人類が生み出してきた分子の中には構造美を備えた分子が数多くあります。そして、多くの人が美しいと思う分子の多くは、機能も備えています。有機合成化学の醍醐味は、自分で思い描いた美しい分子を自ら合成し、その手に取ることができることにあります。
遷移金属は、炭素と異なった結合数を取ることができます。例えば、1つの遷移金属原子にフェニル基を六つ結合させた、対称性の高い分子を合成しました。分子は数nmのサイズですのでどんなに高倍率の顕微鏡を用いても直接人の目で構造を観測することはできません。我々はX線を用いることで合成した分子の構造を正確に決めることができます。
この技術を使うと、美しい分子を直接目で見ることのみならず、触媒反応における触媒活性種の構造を分子レベルで議論することができます。例えば、1-2, 1-3で紹介したクロスカップリング反応の触媒活性種であるアート型錯体を単離し、構造決定することにより反応機構の詳細を明らかにすることができました。

関連文献
M. Hara, Y. Hirooka, T. Iwasaki, K. Nozaki, Inorg. Chem. 2024, 63, 21474–21487.
T. Iwasaki, Y. Hirooka, H. Takaya, T. Honma, K. Nozaki, Organometallics 2021, 40, 2489–2495.
T. Iwasaki, T. Akaiwa, Y. Hirooka, S. Pal, K. Nozaki, N. Kambe, Organometallics 2020, 39, 3077–3081.
T. Iwasaki, W. Yokoyama, N. Kambe, Organometallics 2019, 38, 2701–2704.
T. Iwasaki, A. Fukuoka, X. Min, W. Yokoyama, H. Kuniyasu, N. Kambe, Org. Lett. 2016, 18, 4868–4871.
3. イオンが織りなす触媒機能
有機溶媒中ではイオン結合を形成するイオン同士は比較的近接して存在すると考えられます。実際に、1-2, 1-3で述べたアート型錯体によるクロスカップリング反応では遷移金属アニオンのみならずマグネシウム対カチオンが酸素やフッ素原子に相互作用することで結合の切断過程に重要な役割を果たしていますし、2で述べた錯体でもリチウムカチオンが動的に相互作用することが分かっています。
私たちは近接したカチオンとアニオンがそれぞれ触媒機能を持てば、イオン結合によって緩く繋がった触媒反応場を生み出せると考えて研究を進めています。そこで注目したのは、これまで遷移金属触媒の分子設計であまり注目されてこなかった対アニオンです。通常、対アニオンは触媒に用いられる遷移金属塩が元から備えているハロゲン化物イオンや金属への相互作用を弱くするために安定アニオンが用いられますので、これらの対アニオンは触媒機能を持ちません。
三配位ホウ素をルイス酸点として有するアニオン性の四配位ホウ素化合物を新たに設計・合成しました。これをカチオン性イリジウム触媒の対アニオンに用いると、ルイス塩基性置換基を二つ有するベンゼンの炭素―水素結合の切断反応が効率よく進行し、汎用の安定アニオンを有するイリジウム触媒に比べて触媒活性が8倍以上に向上することを明らかにしました。
ルイス酸以外の機能を対アニオンに導入すべく検討を進めています。
関連文献
R. Mandai, T. Iwasaki, K. Nozaki, Angew. Chem. Int. Ed. accepted.